(二)学习物质的低级思维办法时形成的化学理论或得到的方法
VII、利用元素周期表及其补充:共价键的键能、电离常数;原子、分子、晶体构造推出物质性子的方法

即图2(化学的高等基本思维办法)中的赤色部分:
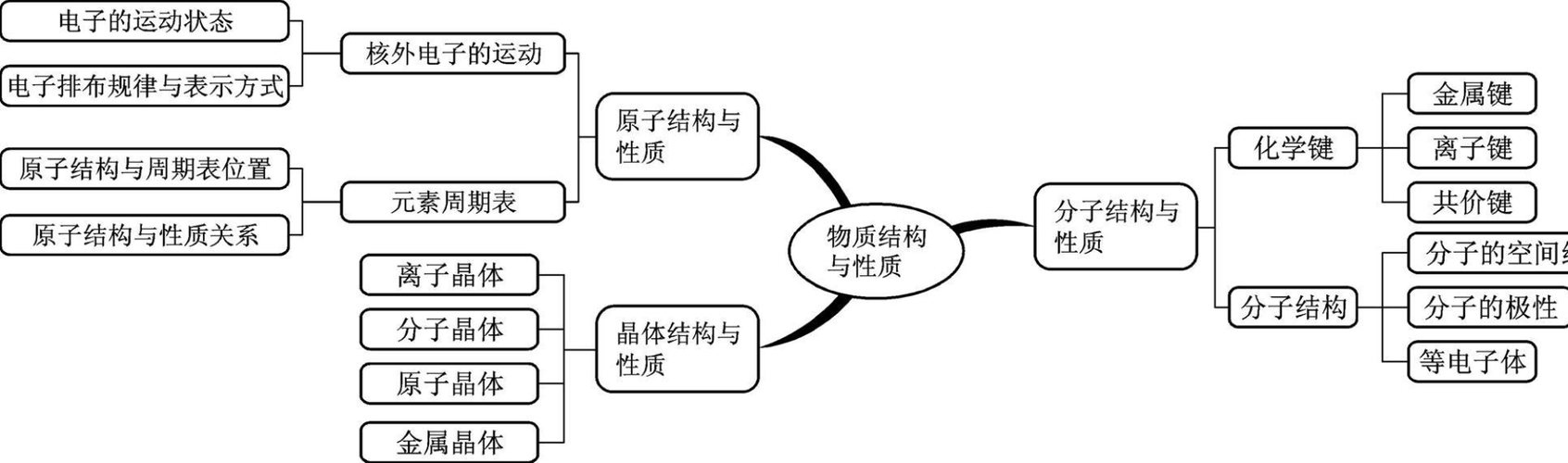
三、推出物质性子的方法
(一)由物质构造、元素周期表推出物质的物理性子的方法:
物理性子:不须要通过化学变革表示的性子。包括:物质本身固有的性子:某条件下,物质的颜色、光泽、状态、气味(生物浸染)、密度;通过物理变革表示的性子:溶解性或溶解度、熔点、沸点、挥发性、硬度、导电性、传热性、延展性。
1.由物质构造推出其物理性子的方法:
(1)利用相似相溶事理,根据分子的极性推出物质的溶解性的方法:
水分子是极性分子,由非极性分子组成的物质难溶于水,如氢气、氮气、氧气、甲烷、四氯化碳等;氯气、溴单质、碘单质、二氧化碳等在水中溶解度不大。极性越靠近水分子的极性的分子越易溶于水,如氨气、氟化氢(氨气、氟化氢分子与水分子之间还存在氢键)、氯化氢、溴化氢、碘化氢等。
有机溶剂的分子或极性较小,如乙醇、氯仿即三氯甲烷等,或属于非极性分子,如苯、四氯化碳等,由非极性分子组成的物质易溶于有机溶剂,如氢气、氮气、氧气、甲烷、四氯化碳、氯气、溴单质、碘单质、二氧化碳等。由极性越强的分子组成的物质越难溶于有机溶剂,如氨气、氟化氢(氨气、氟化氢分子与水分子之间还存在氢键)、氯化氢、溴化氢、碘化氢等。
总之,溶剂粒子与溶质粒子之间的浸染力比溶质与溶质、溶剂与溶剂之间的浸染力大越多,溶质就越易溶于溶剂中。
(2)利用每类晶体的共同物理性子,推出所学晶体的水溶性和熔沸点、导电性、传热性、延展性、金属光泽、硬度的方法:
原子晶体的熔沸点高,硬而脆,难溶于水等一样平常溶剂。
离子晶体的熔沸点较高,硬而脆,多数能溶于水,其水溶液和熔融状态能导电。
分子晶体的熔沸点低,多数硬度小且脆。
金属晶体熔沸点差异大,能导电、能传热、有延展性和金属光泽,除活泼金属跟水反应而溶于水外,其它金属难溶于水。
可由物质的熔沸点判断该物质在某温度和某压强下的状态。
(3)根据物质的构造比较物质的熔沸点、硬度和挥发性的方法:
首先要认识,熔化沸腾时,离子晶体毁坏的是离子键;金属晶体毁坏的是金属键;原子晶体毁坏的是共价键;分子晶体毁坏的是分子间浸染力。所要毁坏的相互浸染越强,晶体的熔沸点越高。
A、根据不同类型范例晶体中相互浸染的相对强弱比较不同晶体的熔沸点、硬度等:
原子晶体、离子晶体(或金属晶体)、分子晶体的熔沸点一样平常依次降落,硬度一样平常依次减小,挥发性一样平常依次增强。如范例的原子晶体金刚石、范例的离子晶体氯化钠、相对分子质量不是很大的分子晶体二氧化碳晶体等,它们的熔沸点依次降落,硬度依次减小,挥发性依次增强。但要把稳,由于每类相互浸染都受到许多成分影响,以是其强弱也相差甚远,因此以上规律并非绝对,只对范例的晶体才适用。如,离子晶体MgO的熔沸点比原子晶体的SiO2的高;金属晶体钠、钾、汞等的熔点比分子晶体硫的低。
B、根据影响每类相互浸染强弱的成分与规律比较同类晶体中不同物质的熔沸点、硬度和挥发性:
①离子晶体:阴阳离子带的电荷数越多,阴阳离子半径越小,离子键越强,一样平常,熔沸点越高,硬度越大。由此可推出都属离子晶体的氯化钠的熔点比氯化钾的高,硬度比氯化钾的大。
②金属晶体:金属原子的价电子数越多,金属阳离子半径越小,金属键越强,熔沸点越高,硬度越大,越难挥发。由此可推出都属金属晶体的锂、钠、钾、铷、铯的熔沸点依次降落,硬度依次减小,挥发性依次增强;钠、镁、铝或钾、钙、铁的熔沸点依次升高,硬度依次增大,挥发性依次减弱。
③原子晶体:共价键越短,共价键越强,熔沸点越高,硬度越大,越难挥发。由此可推出都属原子晶体的金刚石、碳化硅、硅晶体的熔沸点依次降落,硬度依次减小,挥发性依次增强。
④分子晶体:
a、分子的组成:氮、氧、氟的氢化物在液态和固态时分子之间存在比较强的氢键,熔沸点比较高,液体比较难挥发。如,熔沸点:NH3>PH3;H2O>H2S;HF>HCl。
b、分子的极性:其他成分相同时,分子的极性越强,分子间浸染力越大,熔沸点比较高,液体比较难挥发。如,熔沸点:NH3>CH4;CO>N2。
c、分子的形状:其他成分相同时,分子的链越直,分子间的间隔越小,分子间浸染力越大,熔沸点比较高,液体比较难挥发。如,熔沸点:正丁烷>异丁烷。
d、相对分子质量:其他成分相同时,相对分子质量越大,分子间浸染力越大,熔沸点比较高,液体比较难挥发。如,熔沸点:硒化氢>硫化氢;一样平常,同系物随着碳原子数增加熔沸点升高。
e、熔点不但受融化时毁坏的相互浸染的强弱影响,而且受构造单元的对程度影响。其相互浸染力相同时,构造单元的对程度越高,晶体的熔点越高。如,熔点:新戊烷>正戊烷>异戊烷;甲烷>乙烷>丙烷等。
其余,金属晶体具有的共性是:能导电、传热、有延展性、有金属光泽。离子晶体在熔融时能导电、传热。
















